 杨冰
杨冰 一、引言
在医学领域,器官移植一直是拯救终末期器官衰竭患者生命的重要手段。然而,器官短缺问题长期困扰着全球医学界,无数患者在等待供体的过程中失去了生命。近年来,异种器官移植逐渐成为研究的热点,其中猪因其器官大小、生理功能与人类接近,成为极具潜力的供体来源。2025年,国内在异种器官移植领域取得了重大突破——全球首例基因编辑猪肝人体移植成功,术后患者存活超100天,这一成果为全球器官短缺问题带来了新的希望。
二、突破的背景与意义
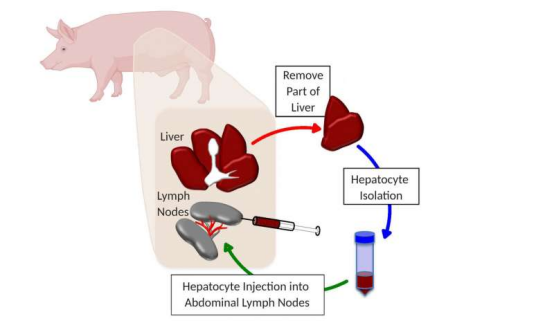
(一)器官短缺的现状
据世界卫生组织(WHO)统计,目前全世界每年约200万人需要器官移植,但全球平均器官供需比不足1:20。在我国,器官短缺问题同样严峻。以肝病为例,我国有近4亿肝病患者,每年新增30万—50万肝衰竭患者。对于肝衰竭,肝移植是一个有效根治方式,但很多人因等不到人类供肝而失去生命。肾脏移植方面,我国终末期肾病患者超100万,每年仅约1万例肾移植手术,大量患者在等待中死亡。
(二)异种器官移植的探索
为了解决器官短缺问题,医学界将目光投向了异种器官移植。猪因其繁殖周期短、器官大小和生理功能与人类接近,被认为是异种器官来源的优选动物。然而,异种器官移植面临着诸多挑战,其中最大的问题是免疫排斥反应。猪的器官表面存在一些抗原,会引发人体的免疫系统攻击,导致移植失败。此外,还存在跨物种病原体传播的风险。
(三)本次突破的意义
此次国内完成的全球首例基因编辑猪肝人体移植,术后患者存活超100天,具有重大的意义。这一成果标志着我国在异种器官移植领域迈入了世界前列,为全球器官短缺问题提供了新的解决方案。如果异种肝移植技术成熟,将不受供肝数量限制,使更多终末期肝病患者获益,未来可能完全替代同种肝移植。
三、手术的实施过程
(一)前期准备
基因编辑猪的培育:此次移植手术使用的基因编辑猪由成都中科奥格生物科技有限公司培育。科研团队通过精准敲除引发超急性和急性血管性排斥的关键抗原(如α-Gal、Sda、Neu5Gc),并转入人源化补体及凝血调节蛋白等,成功将猪肝脏“伪装”成人类器官,大幅降低了免疫风险。这些基因编辑猪一出生就要被送进超洁净猪舍,断奶接受人工饲养,以确保生物安全。
患者的筛选:接受移植的患者是一位终末期肝病患者,在经过严格的评估后,确定其符合移植条件。由于患者病情严重,且没有合适的人类供肝,在患者家属同意的情况下,决定进行基因编辑猪肝人体移植手术。
手术方案的制定:手术方案先后通过了学术委员会、医学伦理委员会、器官移植委员会和动物委员会的论证,严格按照国家有关规定逐项进行。手术由空军军医大学西京医院的多学科专家团队共同参与,包括肝胆外科、麻醉科、外科手术室、超声科、肾脏内科、重症医学科等十余个科室。
(二)手术过程
供体猪肝的获取:手术当天,专家团队从基因编辑猪体内获取全肝。供体猪肝脏重量约800克,经过严格的检测和处理,确保其质量和安全性。
患者原肝的切除与新肝的植入:在麻醉状态下,专家团队对患者进行了原肝切除手术。随后,将基因编辑猪肝原位移植到患者体内,进行动静脉重建、止血关腹等多个步骤。整个手术历时十余个小时,过程复杂而精细。
(三)术后监测与护理
生命体征的监测:术后,患者被送入重症监护室进行密切监测。医护人员实时监测患者的心率、血压、呼吸等生命体征,确保患者的生命安全。
免疫抑制治疗:为了防止免疫排斥反应的发生,患者接受了免疫抑制治疗。医生根据患者的具体情况,调整免疫抑制剂的剂量和种类,以达到理想的免疫抑制效果。
各项指标的检测:定期检测患者的肝功能、肾功能、凝血功能等各项指标,评估移植肝脏的功能和患者的身体状况。
四、术后患者的存活情况
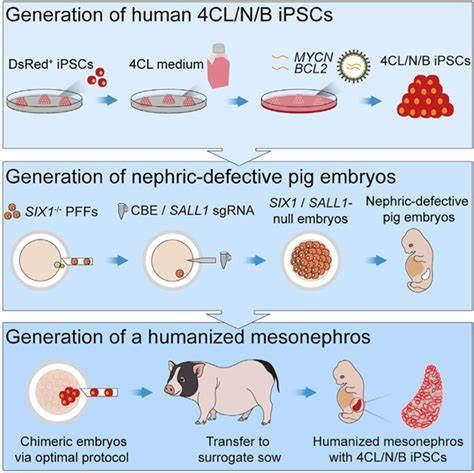
(一)存活超100天的成果
截至目前,接受基因编辑猪肝人体移植的患者术后存活已超100天,创造了全球异种肝移植的存活纪录。在这100多天里,患者的生命体征平稳,肝功能等多项指标基本正常,移植肝脏在人体内能够发挥正常的生理功能。
(二)患者的身体状况
生理指标:患者的血肌酐、转氨酶、胆红素等生理指标持续正常,尿量稳定。这表明移植肝脏的代谢和排泄功能正常,能够有效地清除体内的代谢废物。
生活质量:患者的身体状况逐渐好转,精神状态良好。在医护人员的精心护理下,患者能够进行一些简单的活动和康复训练,生活质量得到了一定的提高。
(三)与全球其他案例的对比
在全球范围内,此前已经进行了一些基因编辑猪器官的人体移植试验,如猪心、猪肾移植等。但猪肝移植由于肝脏的生理功能更为复杂,涉及合成、分解、凝血、解毒和免疫等多种功能,其难度更大。此次国内完成的基因编辑猪肝人体移植,术后患者存活超100天,相比其他案例取得了更为显著的成果。例如,美国进行的猪心移植患者最长存活了2个多月,猪肾移植患者最长存活了4个多月(后因排斥反应被迫摘除),而此次猪肝移植患者的存活时间更长,且各项指标稳定。
五、技术突破的关键因素
(一)基因编辑技术的创新
多基因编辑:此次移植使用的基因编辑猪进行了6种基因编辑,包括敲除了3种会引起人“超急性排斥和急性体液性排斥”的猪抗原,转入了2种“人补体调节蛋白”和1种“人凝血调节蛋白”。这种多基因编辑策略大大降低了猪肝脏的免疫原性,减少了免疫排斥反应的发生。
基因编辑的精准性:科研团队通过先进的基因编辑技术,实现了对猪基因的精准改造。在敲除有害基因的同时,确保了猪肝脏的正常生理功能不受影响。
(二)免疫抑制方案的优化
个性化免疫抑制:西京医院团队根据患者的具体情况,制定了个性化的免疫抑制方案。在术后早期,使用较强的免疫抑制剂来抑制免疫系统的反应,防止超急性排斥反应的发生。随着患者身体的恢复,逐渐调整免疫抑制剂的剂量和种类,以减少药物的副作用。
联合用药:采用了多种免疫抑制剂联合用药的方式,提高了免疫抑制的效果。同时,密切监测患者的免疫状态,及时调整用药方案。
(三)多学科协作的优势
团队的专业性:此次手术由空军军医大学西京医院的多学科专家团队共同参与,包括肝胆外科、麻醉科、外科手术室、超声科、肾脏内科、重症医学科等十余个科室。每个科室的专家都具有丰富的临床经验和专业知识,能够为手术的成功提供保障。
协作的紧密性:在手术过程中,各科室之间密切协作,相互配合。从供体猪肝的获取、患者的麻醉、手术的操作到术后的监测和护理,每个环节都紧密相连,确保了手术的顺利进行和患者的安全。
六、面临的挑战与未来展望
(一)面临的挑战
长期安全性:虽然患者术后存活超100天,但异种肝移植的长期安全性仍需要进一步观察和研究。长期来看,可能会出现慢性排斥反应、跨物种病原体传播等问题,需要建立长期的监测和随访机制。
伦理问题:异种器官移植涉及到伦理问题,如动物福利、人类尊严等。在推进异种器官移植临床应用的过程中,需要充分考虑伦理因素,制定相关的伦理准则和规范。
技术普及:目前,基因编辑猪肝人体移植技术还处于研究阶段,技术难度大,成本高。要实现技术的普及和应用,还需要进一步降低成本,提高技术的可重复性和稳定性。
(二)未来展望
临床试验的推进:随着技术的不断成熟,未来有望开展更大规模的临床试验,进一步验证基因编辑猪肝人体移植的安全性和有效性。通过临床试验,积累更多的临床数据,为技术的临床应用提供依据。
技术的优化与创新:科研人员将继续对基因编辑技术和免疫抑制方案进行优化和创新,提高异种肝移植的成功率和患者的生存质量。例如,探索更有效的基因编辑方法,开发新型的免疫抑制剂等。
解决器官短缺问题:如果异种肝移植技术最终能够成功应用于临床,将为全球器官短缺问题带来根本性的解决方案。更多的终末期肝病患者将有机会获得移植治疗,重获新生。
七、结论
国内完成的全球首例基因编辑猪肝人体移植,术后患者存活超100天,是异种器官移植领域的重大突破。这一成果不仅为全球器官短缺问题提供了新的希望,也展示了我国在医学科技领域的创新能力和实力。然而,我们也应该清醒地认识到,异种肝移植技术还面临着诸多挑战,需要科研人员、医护人员、伦理学家等各方共同努力,不断推进技术的研究和应用。相信在不久的将来,异种肝移植技术将更加成熟,为更多的患者带来福音。





















