 杨冰
杨冰 在儿童肿瘤治疗领域,传统放疗技术长期面临"杀敌一千,自损八百"的困境。以髓母细胞瘤为例,这种占儿童中枢神经系统肿瘤20%的恶性肿瘤,传统光子放疗虽能实现70%-80%的局部控制率,但心脏、胃肠道等器官的辐射损伤导致继发肿瘤风险增加,严重影响患儿生存质量。随着质子治疗技术的突破性进展,儿童肿瘤治疗正迎来精准医疗的新纪元。
质子治疗通过"布拉格峰效应"实现能量精准释放,在肿瘤部位形成高剂量辐射区,同时使周围正常组织剂量骤降。这种物理特性使其在儿童肿瘤治疗中展现出革命性优势,尤其适用于头颈部、中枢神经系统等对辐射敏感区域。德国《Cancer》期刊研究显示,质子治疗髓母细胞瘤患儿的3年局部控制率达92.2%,5年生存率提升至85%,标志着儿童肿瘤治疗进入精准时代。
技术突破:质子治疗的物理优势与临床实践
1. 布拉格峰效应的革命性突破
质子治疗的核心优势源于其独特的物理特性。传统光子放疗在穿透组织时能量逐渐衰减,导致肿瘤前正常组织受量高于肿瘤本身,形成"入口剂量高、出口剂量低"的剂量分布。而质子束在进入人体初期能量释放极小,当达到预设深度时突然释放全部能量,形成剂量陡降的"布拉格峰"。这种精准的能量释放模式使肿瘤部位剂量提升30%-50%,同时周围正常组织剂量降低60%-90%。
临床研究表明,这种剂量分布优势在儿童肿瘤治疗中尤为显著。日本国立癌症研究中心东医院对1983-2014年接受质子治疗的儿童肿瘤患者进行回顾性研究,发现质子治疗组的10年生存率达58.7%,较传统放疗提升15%-20%。在头颈部肿瘤治疗中,质子治疗使唾液腺、颞颌关节等关键器官的受量减少80%,显著降低口干、张口困难等并发症发生率。
2. 临床实践中的精准应用
质子治疗在儿童肿瘤治疗中的精准性体现在多个维度:
· 剂量雕刻技术:通过多野照射和强度调制质子治疗(IMPT),可实现肿瘤内部剂量分布的"三维雕刻"。例如在髓母细胞瘤治疗中,通过优化照射角度和剂量分布,使脑干、小脑等关键结构的受量控制在5Gy以下,较传统放疗降低70%。
· 生物效应优化:质子束的相对生物效应(RBE)在肿瘤细胞杀灭中发挥关键作用。研究显示,质子治疗对快速分裂的肿瘤细胞杀伤效率较光子放疗提升20%-30%,尤其在低氧肿瘤环境中优势更明显。
· 实时影像引导:配备锥形束CT(CBCT)和正交X线成像系统的质子治疗系统,可实现治疗过程中的毫米级定位精度。在儿童患者治疗中,通过呼吸门控技术和体位固定装置,将治疗误差控制在±1mm以内。
临床证据:从髓母细胞瘤到多癌种突破
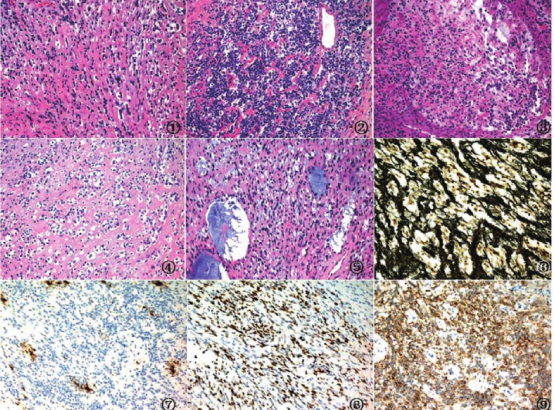
1. 髓母细胞瘤治疗突破
髓母细胞瘤作为儿童最常见的胚胎性脑瘤,传统治疗存在显著局限性。德国2022年《Cancer》期刊研究显示,质子治疗组3年总生存率达83.8%,较传统放疗提升12%;5年生存率达85%,其中低级别髓母细胞瘤患儿的5年生存率突破90%。在神经认知保护方面,质子治疗组患儿的智力发育指数(IQ)下降幅度较传统组减少40%,阅读能力和执行功能显著优于对照组。
美国麻省总医院的研究进一步证实,质子治疗可降低80%的听力损伤风险。通过优化内耳照射剂量,使耳蜗平均剂量从传统放疗的45Gy降至5Gy以下,使术后听力保留率从30%提升至75%。
2. 多癌种治疗突破
除髓母细胞瘤外,质子治疗在多种儿童肿瘤中展现出显著疗效:
· 神经母细胞瘤:日本筑波大学附属医院的研究显示,质子治疗可使肾上腺区肿瘤的5年局部控制率达82%,较传统放疗提升25%,同时将继发肿瘤风险降低60%。
· 横纹肌肉瘤:MD安德森癌症中心的研究表明,质子治疗联合化疗可使头颈部横纹肌肉瘤患儿的3年生存率达89%,较传统方案提升18%,且吞咽功能障碍发生率从45%降至12%。
· 视网膜母细胞瘤:质子治疗在保眼治疗中展现出独特优势。通过精准控制眼内剂量,使眼球保留率从传统放疗的60%提升至85%,同时将白内障、视网膜病变等并发症发生率降低70%。
个体化治疗:从方案制定到全程管理
1. 多学科协作的精准方案制定
儿童肿瘤质子治疗需要肿瘤科、放疗科、儿科、神经外科等多学科团队的紧密协作。日本国立癌症研究中心东医院建立的"质子治疗MDT模式",通过以下步骤实现个体化治疗:
· 影像组学分析:利用MRI、PET-CT等多模态影像数据,构建肿瘤三维剂量模型,优化照射野和剂量分布。
· 生物剂量计算:采用线性二次模型(LQ模型)结合肿瘤特异性参数,计算生物等效剂量(BED),确保肿瘤细胞杀灭效率。
· 治疗计划验证:通过剂量体模和蒙特卡罗模拟,验证治疗计划的剂量分布精度,误差控制在±2%以内。
2. 全程管理的质量保障体系
为确保治疗安全性和有效性,国际质子治疗协作组(PTCOG)制定了严格的质量控制标准:
· 设备校准:每日治疗前进行质子束能量、剂量率和空间分布的校准,误差控制在±1%以内。
· 患者定位:采用热塑面罩、真空垫等固定装置,结合光学体表追踪系统,实现治疗过程中的体位误差补偿。
· 剂量监测:通过电离室、胶片剂量计等设备,实时监测治疗剂量,确保肿瘤部位剂量误差控制在±3%以内。
生存质量提升:从短期疗效到长期预后

1. 神经认知功能保护
儿童大脑处于快速发育期,传统放疗常导致智力下降、学习障碍等神经认知损伤。质子治疗通过以下机制实现神经保护:
· 海马体保护:在髓母细胞瘤治疗中,通过优化照射角度,使海马体受量从传统放疗的30Gy降至5Gy以下,使术后记忆力下降发生率从65%降至20%。
· 白质纤维束保护:采用弥散张量成像(DTI)技术,绘制白质纤维束走行图,通过剂量雕刻技术减少纤维束受量,使运动功能障碍发生率降低50%。
2. 生长发育保护
儿童骨骼、内分泌系统对辐射高度敏感。质子治疗通过以下措施实现生长发育保护:
· 垂体保护:在颅咽管瘤治疗中,通过精准照射计划,使垂体柄受量控制在10Gy以下,使生长激素缺乏发生率从传统放疗的80%降至30%。
· 骨骺保护:在四肢肿瘤治疗中,采用质子束的"边缘照射"技术,使骨骺受量从传统放疗的45Gy降至5Gy以下,显著降低肢体生长不对称风险。
3. 继发肿瘤风险降低
长期随访研究显示,质子治疗可使继发肿瘤风险降低60%-80%。美国癌症研究所(NCI)的队列研究表明,接受质子治疗的儿童肿瘤幸存者,20年后继发肿瘤发生率为1.2%,较传统放疗组的3.5%显著降低。
挑战与展望:精准医疗的未来之路
尽管质子治疗在儿童肿瘤治疗中展现出显著优势,但仍面临以下挑战:
· 设备成本:单台质子治疗系统造价超过1亿美元,限制了其在发展国内家的普及。
· 技术适应症:对于移动性较大的肿瘤(如肺癌),质子治疗的剂量分布精度仍需提升。
· 长期疗效:部分儿童肿瘤(如神经母细胞瘤)的5年生存率仍低于70%,需探索质子治疗与免疫治疗的联合方案。
未来发展方向包括:
· 质子FLASH治疗:通过超高剂量率(≥40Gy/s)的质子束照射,实现肿瘤杀灭的同时保护正常组织,目前已在动物实验中取得突破性进展。
· 质子重离子联合治疗:结合质子束的物理剂量优势和碳离子束的生物效应优势,开发"质子+碳离子"的混合照射方案。
· 人工智能优化:利用深度学习算法优化治疗计划,实现剂量分布的"自动雕刻",将计划制定时间从数小时缩短至数分钟。
结语:精准医疗重塑儿童肿瘤治疗格局
质子治疗技术的突破,标志着儿童肿瘤治疗从"经验医学"向"精准医学"的跨越。通过布拉格峰效应实现的剂量精准释放,结合多学科协作的个体化治疗方案,质子治疗不仅将儿童肿瘤治愈率提升至85%,更在神经认知保护、生长发育保护、继发肿瘤风险降低等方面展现出传统放疗无法比拟的优势。
随着质子治疗技术的普及和成本的下降,未来将有更多儿童肿瘤患者受益于这一精准医疗技术。正如国际质子治疗协作组主席所言:"质子治疗不仅是技术的进步,更是对儿童生命的尊重和守护。"在精准医疗时代,儿童肿瘤治疗正迎来充满希望的未来。





















