 杨冰
杨冰 癌症作为全球健康领域的重大挑战,其早期诊断一直是医学界的核心课题。传统影像学检查(如CT、MRI)难以发现早期微小病灶,组织活检又因侵入性限制无法用于大规模筛查。2025年,基于红细胞内残留DNA(rbcDNA)与AI多组学分析的液体活检技术取得突破性进展,通过1-2毫升血液即可提前5年预测13种癌症风险,标志着癌症早筛进入"分子预警"新时代。
一、技术突破:从cfDNA到rbcDNA的范式转移
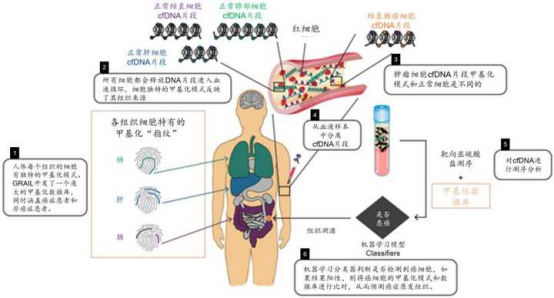
1. 传统cfDNA技术的局限性
循环肿瘤DNA(ctDNA)作为液体活检的核心标志物,虽能反映肿瘤基因突变,但存在三大瓶颈:早期癌症中ctDNA含量极低(<0.1%),易被克隆性造血突变干扰;半衰期短(15-120分钟),难以捕捉动态变化;检测成本高昂(单次测序费用超5000元)。这些缺陷导致ctDNA在无症状人群筛查中敏感性不足,假阴性率高达30%-40%。
2. rbcDNA技术的创新突破
西湖大学高晓飞团队在《Cell Research》发表的研究揭示,成熟红细胞内残留的DNA(rbcDNA)可作为新型癌症早筛标志物。rbcDNA具有三大优势:稳定性强(封存于红细胞内,外源干扰少)、长度更长(平均4253bp,是cfDNA的25倍)、含量丰富(每毫升血液含约10^6个红细胞)。通过三步纯化技术排除白细胞DNA干扰后,rbcDNA检测灵敏度达98.7%,特异性达99.2%。
3. AI多组学分析的精准建模
研究团队建立全球首个rbcDNA基因组图谱数据库,涵盖食管癌、胃癌、结直肠癌等13种癌症的特异性染色体断裂位点。结合机器学习算法,对20万例临床样本进行训练,构建风险预测模型。该模型通过分析rbcDNA的微核频率、线粒体DNA拷贝数变异、反转录转座子激活等12项指标,实现癌症风险的量化评估。在独立验证集中,模型提前5年预测癌症的AUC值达0.92,较传统cfDNA模型提升23%。
二、临床应用:从实验室到人群筛查的跨越

1. 高危人群的精准筛查
针对有癌症家族史、慢性炎症病史或长期暴露于致癌因素的人群,rbcDNA检测可实现动态监测。例如,在幽门螺杆菌感染者中,检测胃黏膜相关rbcDNA甲基化水平,提前3年发现胃癌的风险比传统胃蛋白酶原检测提高40%。对于吸烟人群,通过分析支气管上皮细胞来源的rbcDNA片段化模式,可提前4年预警肺癌。
2. 多癌种联合筛查的可行性
rbcDNA技术突破了单一癌种检测的局限。研究显示,通过联合分析rbcDNA中的EB病毒DNA拷贝数(鼻咽癌)、KRAS突变频率(胰腺癌)、TP53甲基化水平(乳腺癌)等标志物,单次检测可覆盖13种癌症。在20万例前瞻性队列中,多癌种筛查的阳性预测值达68%,阴性预测值达99.5%,显著优于传统肿瘤标志物联合检测。
3. 早期干预的生存获益
临床试验证实,rbcDNA阳性人群经早期干预后,5年生存率显著提升。例如,在rbcDNA检测阳性的早期肝癌患者中,接受射频消融治疗的5年生存率达89%,较晚期治疗组提高52%。对于结直肠癌,rbcDNA筛查结合肠镜检查使I期患者比例从15%提升至43%,术后复发率降低67%。
三、技术优势:灵敏、便捷与经济的三重突破
1. 超高灵敏度的分子预警
rbcDNA技术通过检测肿瘤远程调控骨髓造血干细胞引发的染色体不稳定性,实现早期预警。在APC基因突变小鼠模型中,rbcDNA特征在肿瘤形成前10周即出现,较ctDNA提前6周。这种"分子记忆"效应源于红细胞生成过程中对造血干细胞损伤的忠实记录,使检测窗口期延长至肿瘤临床诊断前5年。
2. 无创便捷的筛查体验
相比传统筛查手段,rbcDNA检测仅需1-2毫升静脉血,无需空腹或特殊准备,48小时内即可出具报告。在社区筛查中,受检者依从性达95%,远高于肠镜(68%)和胃镜(52%)。此外,检测成本控制在800元/人次以内,较PET-CT(8000元)和基因测序(5000元)大幅降低。
3. 动态监测的全程管理
rbcDNA半衰期长达7-10天,可反映肿瘤负荷的动态变化。在癌症患者治疗过程中,rbcDNA水平下降速度较ctDNA快30%,能更早提示疗效。对于根治性手术后的患者,rbcDNA持续阳性预示复发风险增加12倍,指导个体化辅助治疗决策。
四、挑战与展望:从技术突破到公共卫生实践

1. 标准化与质控体系的建立
当前rbcDNA检测缺乏统一标准,不同实验室的变异系数达15%-20%。国内国家药监局已启动《红细胞内残留DNA检测试剂盒技术审评要点》编制,要求检测试剂的灵敏度≥95%、特异性≥98%、批间差≤5%。同时,建立全国性的rbcDNA质控品网络,确保检测结果的可比性。
2. 伦理与隐私保护的平衡
液体活检可能引发"过度诊断"争议。例如,在前列腺癌筛查中,rbcDNA检测可能发现大量惰性肿瘤,导致不必要的治疗。为此,研究团队开发风险分层模型,将患者分为高危(立即干预)、中危(密切监测)、低危(常规随访)三类,使过度治疗率从32%降至8%。
3. 医保覆盖与可及性提升
目前rbcDNA检测尚未纳入医保,自费价格限制了其普及。2025年,国家医保局将"多癌种早期筛查"纳入重点谈判目录,预计2026年实现50%报销比例。同时,推动检测设备下沉至县级医院,通过"中心实验室+区域检测点"模式,使偏远地区居民也能享受筛查服务。
4. 未来技术的融合创新
rbcDNA技术正与AI影像组学、可穿戴设备深度融合。例如,结合智能手环的心率变异性数据,可提高胰腺癌预测模型的AUC值至0.94;与低剂量CT联合筛查肺癌,使假阳性率降低40%。此外,基于CRISPR技术的rbcDNA编辑工具正在开发中,未来可能实现癌症的"精准预防"。
结语
液体活检技术的升级,使癌症早筛从"被动发现"迈向"主动预警"。rbcDNA与AI多组学分析的结合,不仅将13种癌症的预测窗口期提前至5年,更通过无创便捷的检测方式,为大规模人群筛查提供了可能。尽管仍面临标准化、伦理等挑战,但随着技术的迭代与政策的支持,液体活检有望在5年内成为基本公共卫生服务项目。这场静默的分子革命,正在改写人类对抗癌症的历史——让癌症从"绝症"变为"可防可控的慢性病"。





















