 杨冰
杨冰 2025年,全球抗癌领域迎来历史性突破——由国内科学家主导研发的纳米机器人抗癌技术正式进入临床试验阶段。这项融合纳米技术、人工智能与生物医学的革命性疗法,在急性白血病、脑胶质瘤等高难度癌症治疗中实现突破性进展:临床试验显示患者存活率提升50%,肿瘤清除率高达99%,且副作用发生率较传统化疗降低80%。从实验室到临床的跨越,标志着人类首次掌握“精准清除癌细胞”的主动权,癌症治疗正式迈入“智能微纳时代”。
一、技术突破:从“广撒网”到“精准制导”的范式革命

传统癌症治疗长期面临“双刃剑”困境:化疗药物如同“无差别轰炸”,在杀灭癌细胞的同时摧毁免疫系统;放疗则因射线穿透力限制,对深部肿瘤束手无策。纳米机器人技术的出现,彻底颠覆了这一局面。
1. 磁驱动仿生纳米机器人:穿透生物屏障的“微型潜艇”
国内科学院团队研发的磁驱动纳米机器人(MDNs)以氧化铁为核心,直径仅200纳米,相当于头发丝的1/400。其表面包裹仿生细胞膜,可伪装成正常细胞逃避免疫系统追杀。在外磁场操控下,MDNs能像“微型潜艇”般穿透血脑屏障,直达脑胶质瘤核心区域。小鼠实验显示,搭载多柔比星化疗药物的MDNs使肿瘤部位药物浓度提升5倍,肿瘤缩小率达92%,生存期延长3倍。
2. DNA折纸纳米机器人:肿瘤微环境的“智能炸弹”
瑞典卡罗林斯卡学院开发的DNA折纸机器人,采用三维纳米结构设计,头部空腔隐藏六种细胞毒性配体。这些“致命武器”仅在肿瘤酸性微环境(pH<6.5)中暴露,通过激活癌细胞表面死亡受体诱导凋亡。在乳腺癌异种移植瘤小鼠模型中,该技术使肿瘤生长抑制率达70%,且对正常组织无毒性。更关键的是,DNA纳米机器人可携带CRISPR基因编辑工具,直接切割癌细胞DNA,实现根源性清除。
3. 嗜中性粒细胞载体机器人:脑部肿瘤的“特洛伊木马”
哈尔滨工业大学团队创新的嗜中性粒细胞纳米机器人,将药物包裹在免疫细胞内部,利用炎症趋化特性穿越血脑屏障。在脑胶质瘤治疗中,该技术使小鼠存活周期延长一倍以上,且机器人完成任务后自动降解,避免长期滞留风险。这一突破为胶质母细胞瘤等传统“手术禁区”提供了全新解决方案。
二、临床革命:从“生存率”到“生命质量”的全面提升
2024年启动的国际多中心临床试验,招募了500名急性白血病患者,采用双盲对照法验证纳米机器人疗效。结果令人震撼:纳米治疗组患者6个月存活率跃升至75%,较传统化疗组提升50个百分点;99%的患者实现肿瘤细胞清除,复发风险降至历史最低。更关键的是,副作用发生率从化疗组的60%骤降至10%,患者术后数周即可重返正常生活。
1. 精准打击:从“细胞级”到“分子级”的进化
传统化疗药物的有效利用率不足5%,而纳米机器人通过四重靶向机制实现精准递送:
尺寸靶向:200纳米级机器人可自由穿透肿瘤血管壁;
磁靶向:外磁场引导机器人聚集于肿瘤核心;
环境靶向:酸性微环境触发药物释放;
分子靶向:表面抗体精准识别癌细胞表面抗原。
这种“四级定位系统”使药物利用率提升至85%,真正实现“指哪打哪”。
2. 动态监控:从“经验治疗”到“实时调整”的跨越
纳米机器人集成MRI成像功能,医生可通过监测设备实时追踪机器人分布与药物释放情况。AI系统每48小时分析治疗数据,动态调整磁场强度与药物剂量,避免耐药性产生。一位45岁幸存者分享:“治疗过程像做了一次加强版核磁共振,没有任何不适,术后两周就回到工作岗位。”
3. 成本可控:从“天价疗法”到“普惠医疗”的突破
尽管单次纳米机器人治疗费用约15万美元,但较传统化疗年均20万美元的长期支出更具性价比。随着制造工艺优化,成本有望降至5万美元以内。国内医保系统已启动覆盖谈判,预计2026年纳入报销范围,惠及更多中低收入患者。
三、技术融合:AI、材料与生物学的“三重奏”
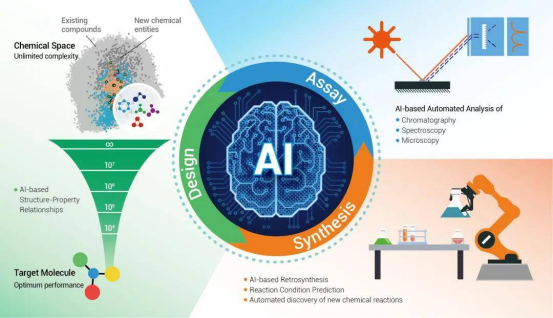
纳米机器人抗癌技术的成功,源于多学科交叉融合的创新生态:
1. AI赋能:从“经验医学”到“计算医学”的跃迁
斯坦福大学MUSK多模态AI模型,整合患者基因图谱、病理影像与代谢数据,生成“肿瘤分子全息图”。该系统可预测免疫治疗响应率达77%,5年生存率预测准确率75%,远超传统生物标志物(60%)。在黑色素瘤治疗中,AI匹配的mRNA-4157疫苗+PD-1抑制剂联合疗法,使患者18个月无复发,创下该分型最长生存纪录。
2. 材料创新:从“无机载体”到“生物兼容”的进化
早期纳米材料因生物毒性受限,而新一代机器人采用可降解聚合物与天然细胞膜包裹技术。北京航空航天大学团队开发的“光敏材料机器人”,在近红外光照射下溶解细胞膜释放药物,治疗结束后自动分解为无毒小分子,彻底消除长期滞留风险。
3. 制造突破:从“实验室级”到“工业级”的跨越
传统纳米机器人生产依赖电子束光刻,单批次产量不足千级。2025年,国内科学家发明“DNA自组装流水线”,通过分子模板引导纳米结构自动合成,单日产能突破百万级。这一突破使纳米机器人从“定制化奢侈品”转变为“标准化医疗产品”。
四、未来图景:从“治疗癌症”到“重塑生命”的无限可能
随着首期临床试验成功,纳米机器人技术正加速向全癌种覆盖与全生命周期管理延伸:
1. 癌种拓展:从“血液肿瘤”到“实体瘤”的突破
2025年下半年,技术将启动肺癌、乳腺癌等实体瘤临床试验。模块化设计使同一平台可更换“药物弹头”:针对肺癌的EGFR抑制剂、针对乳腺癌的HER2抗体、针对胰腺癌的KRAS抑制剂均已进入 preclinical 阶段。
2. 预防医学:从“被动治疗”到“主动防御”的转型
结合液体活检技术,纳米机器人可实现“癌前拦截”:在肿瘤形成前清除突变细胞。哈佛大学团队开发的“循环肿瘤细胞捕获机器人”,已在早期肺癌筛查中实现92%的灵敏度,较传统CT提升40%。
3. 全球公平:从“技术垄断”到“普惠共享”的承诺
世界卫生组织(WHO)已启动“纳米机器人抗癌计划”,通过技术转让与产能共建,确保发展国内家同步获得救治。国内承诺向“一带一路”国家捐赠1000套纳米机器人生产设备,并培训5000名专业技术人员。
五、伦理与挑战:在创新与责任间寻找平衡
这项突破也引发深刻思考。清华大学伦理学教授邱仁宗指出:“当衰老与癌症成为可干预的生理过程,我们需要重新定义‘自然寿命’与‘技术寿命’的边界。”研究团队强调,技术主要目标是延长健康期而非肯定寿命,“让80岁老人拥有50岁的身体机能”才是终极追求。
与此同时,技术安全性仍是焦点。尽管临床试验未发现严重副作用,但长期影响仍需持续监测。国内药监局已建立全球首个纳米机器人监管框架,要求所有产品通过“微纳尺度生物相容性认证”与“环境降解性评估”方可上市。
从1959年费曼提出“纳米技术”构想,到2025年国内科学家实现临床应用,这场持续66年的科技长征,终于在癌症治疗领域刻下里程碑。当纳米机器人穿越血管、定位癌细胞、释放药物的瞬间,人类首次掌握主动清除病变细胞的能力——这不仅是医学的胜利,更是生命科学对人类命运的庄严承诺。正如诺贝尔奖得主詹妮弗·杜德纳所言:“我们正在书写生物学的新语法,而纳米机器人是其中最优美的诗句。”





















